Care sunt cele trei tipuri de radiații nucleare
 Share
Share
Radiatie nucleara se referă la procese prin care nucleele instabile devin mai stabile prin emisia de particule energetice. Cele trei tipuri de radiații nucleare se referă la radiațiile alfa, beta și gamma. Pentru a deveni stabil, un nucleu poate emite o particulă alfa (un nucleu de heliu) sau o particulă beta (un electron sau un pozitron). Adesea, pierderea unei particule în acest fel părăsește nucleul într-un starea excitat. Apoi, nucleul eliberează excesul de energie sub forma unui foton cu raze gama.
Introducere
O problemă este în cele din urmă formată din atomi. Atomii, la rândul lor, sunt alcătuite din protonii, neutronii și electroni. Protonii sunt încărcați pozitiv și electronii sunt încărcați negativ. Neutronii nu sunt taxați. Protonii și neutronii locuiesc în interiorul lui nucleu a atomului, iar protonii și neutronii sunt numiți împreună nucleoni. Electronii se găsesc într-o regiune în jurul nucleului, care este mult mai mare decât dimensiunea nucleului în sine. În atomii neutri, numărul de protoni este egal cu numărul de electroni. În atomii neutri, taxele pozitive și negative se anulează reciproc, dând o taxă netă zero.

Structura atomului - Nucleul se regăsește în regiunea centrală. În regiunea gri, electronul poate fi găsit.
Proprietățile protonilor, neutronilor și electronilor
| particulă | Clasificarea particulelor | Masa | Încărca |
Proton ( ) ) | baryon |  |  |
neutron ( ) ) | baryon |  |  |
electron ( ) ) | leptoni |  |  |
Rețineți că neutronul este puțin mai greu decât protonul.
- ionii sunt atomi sau grupuri de atomi care au pierdut sau au câștigat electroni, făcându-i să aibă o încărcare netă pozitivă sau negativă. Fiecare element este alcătuită dintr-o colecție de atomi având același număr de protoni. Numărul de protoni determină tipul atomului. De exemplu, atomii de heliu au 2 protoni, iar atomii de aur au 79 de protoni.
- izotopi a unui element se referă la atomi care au același număr de protoni, dar un număr diferit de neutroni. De exemplu: protium, deuteriu și tritiu sunt toți izotopii hidrogenului. Toți au fiecare câte un proton. Protium, totuși, nu are neutroni. Deuteriul are un neutron, iar tritiuul are două.
- Număr atomic (număr proton) (
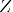 ): numărul de protoni din nucleul unui atom.
): numărul de protoni din nucleul unui atom. - Număr neutru: Numărul de neutroni din nucleul unui atom.
- Nucleon Number (
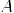 ): Numărul de nucleoni (protoni + neutroni) în nucleul unui atom.
): Numărul de nucleoni (protoni + neutroni) în nucleul unui atom.
Notație pentru reprezentarea nucleelor
Nucleii unui izotop sunt deseori reprezentați în următoarea formă:

De exemplu, izotopii hidrogenului antium, deuteriu și tritiu sunt scrise cu următoarea notație:
 ,
,  ,
,  .
.
Uneori, numărul de proton este, de asemenea, emis și numai simbolul și numărul nucleon sunt scrise. de exemplu.,
 ,
,  ,
,  .
.
Nu există nici o problemă în faptul că nu se afișează explicit numărul de protoni, deoarece numărul de protoni determină elementul (simbolul). Uneori, un anumit izotop poate fi referit la numele elementului și numărul nucleonului, de ex. uraniu-238.
Masa Atomică Unificată
Masa atomică unificată ( ) este definit ca
) este definit ca  masa unui atom de carbon-12.
masa unui atom de carbon-12.  .
.
Cele trei tipuri de radiații nucleare
Alfa Beta și radiația gamma
După cum am menționat mai devreme, cele trei tipuri de radiații nucleare sunt radiațiile alfa, beta și gamma. În alfa radiații, un nucleu devine mai stabil prin emisia a doi protoni și doi neutroni (un nucleu de heliu). Există trei tipuri de radiații beta: beta minus, beta plus și captură electronică. În beta minus radiații, un neutron se poate transforma într-un proton, eliberând un electron și un antineutrino de electroni în proces. În beta plus radiații, un proton se poate transforma intr-un neutron, oferind un pozitron si un antineutrino de electroni. În captarea electronilor, un proton din nucleu captează un electron al atomului, transformându-se într-un neutron și eliberând un neutrino-electron în proces. Gama de radiații se referă la emisia de fotoni de raze gama de către nuclei în stări excitate, pentru ca aceștia să devină excitați.
Ce este Radiația Alpha
În alfa radiații, un nucleu instabil emite un alfa particule, sau a heliu nucleu (adică 2 protoni și 2 neutroni), pentru a deveni un nucleu mai stabil. O particulă alfa poate fi desemnată ca  sau
sau  .
.
De exemplu, un nucleu de poloniu-212 suferă o descompunere alfa pentru a deveni un nucleu de plumb-208:

Când decăderile nucleare sunt scrise în această formă, numărul total de nucleoni de pe partea stângă trebuie să fie egal cu numărul total de nucleoni de pe partea dreaptă. De asemenea, numărul total de protoni din partea stângă trebuie să fie egal cu numărul total de protoni din partea dreaptă. În ecuația de mai sus, de exemplu, 212 = 208 + 4 și 84 = 82 + 2.
Fiul fiicei produs de o degradare alfa, prin urmare, are doi protoni și patru nucleoni mai puțin decât nucleul părinte.
În general, pentru decăderea alfa, putem scrie:

Particulele alfa emise în decăderea alfa au energii specifice, determinate de diferența de masă dintre nucleele părinte și fiice.
Exemplul 1
Scrieți ecuația pentru degradarea alfa a americium-241.
Americium are un număr atomic de 95. În timpul decăderii alfa, nucleul american ar emite o particulă alfa. Noul nucleu produs (nucleul fiicei) ar avea două protoni mai puțin și cu patru nucleoni mai puțin. adică ar trebui să aibă un număr atomic 93 și un număr de nucleon 237. Numărul atomic 93 se referă la un atom de neptuniu (Np). Deci, scriem,

Ce este radiația beta
În radiația beta, un nucleu se descompune prin emițarea unui electron sau a unui pozitron (un pozitiv este antiparticulă din electron, având aceeași masă, dar încărcarea opusă). Nucleul nu conține electroni sau positroni; așa că mai întâi trebuie să se transforme un proton sau un neutron, așa cum vom vedea mai jos. Atunci când un electron sau un positron este eliberat, pentru a conserva numărul de lepton, se eliberează un neutrino electron sau un antineutrino de electroni. Energia particulelor beta (care se referă fie la electroni, fie la positroni) pentru o anumită decădere ar putea lua o serie de valori, în funcție de cantitatea de energie eliberată în timpul procesului de dezintegrare a neutrinului / antineutrino-ului. În funcție de mecanismul implicat, există trei tipuri de radiații beta: beta minus, beta plus și captură electronică.
Ce este Radiația Beta Minus
A beta minus ( ) particulă este un electron. În decăderea beta-minus, un neutron se descompune într-un proton, un electron și un antineutrino de electroni:
) particulă este un electron. În decăderea beta-minus, un neutron se descompune într-un proton, un electron și un antineutrino de electroni:

Protonul rămâne în nucleu în timp ce electronul și electronul antineutrino sunt emise. Procesul Beta minus poate fi rezumat astfel:

De exemplu, aur-202 se descompune de emisia beta minus:

Ce este Radiația Beta Plus
A beta plus ( ) particulă este un pozitron. În decalajul beta plus, un proton este transformat într-un neutron, un pozitron și un neutrino:
) particulă este un pozitron. În decalajul beta plus, un proton este transformat într-un neutron, un pozitron și un neutrino:

Neutronul rămâne în nucleu în timp ce poziția și neutrina electronului sunt emise. Procesul Beta minus poate fi rezumat astfel:

De exemplu, un nucleu de fosfor-30 poate suferi degradare beta plus:

Ce este captarea electronilor
În captarea electronilor, un proton din nucleu "captează" unul dintre electronii atomului, dând un neutron și un neutrino de electroni:

Neutrinul de electroni este emis. Procesul de captare a electronilor poate fi rezumat astfel:

De exemplu, Nichel-59 prezintă decalaj beta plus după cum urmează:

Ce este radiația Gamma
După ce a suferit o descompunere alfa sau beta, nucleul este adesea într-o zonă stare de energie excitat. Aceste nuclee se decuplează prin emiterea unui foton gamma și pierderea excesului de energie. Numărul de protoni și neutroni nu se schimbă în timpul acestui proces. Gama de radiații are de obicei forma:

unde asteriscul reprezintă nucleul într-o stare excitat.
De exemplu, cobalt-60 se poate deforma în nichel-60 prin decăderea beta. Nucleul de nichel format este într-o stare excitat și emite un foton de raze gamma pentru a deveni de-excitat:


Fotoanele emise de razele gamma au, de asemenea, energii specifice în funcție de stările energetice specifice ale nucleului.
Proprietățile Alpha Beta și Gamma Radiation
Comparativ, particulele alfa au cea mai mare masă și încărcătură. Ele se deplasează încet comparativ cu particulele beta și gamma. Aceasta înseamnă că, în timp ce se deplasează prin materie, ei sunt capabili să îndepărteze electonii de particulele de materie, care intră în contact cu mult mai ușor. În consecință, ele au cea mai mare putere ionizantă.
Cu toate acestea, deoarece ele provoacă cel mai ușor ionizarea, ei își pierd, de asemenea, energia cea mai rapidă. În mod obișnuit, particulele alfa pot circula doar cu câteva centimetri în aer înainte de a-și pierde toată energia din particulele de aer ionizant. Particulele alfa nu pot pătrunde nici prin pielea umană, astfel încât acestea să nu poată cauza nici un rău atâta timp cât acestea rămân în afara corpului. Cu toate acestea, dacă un material radioactiv care emit particule alfa este ingerat, acesta poate provoca o mulțime de deteriorări datorită capacității lor puternice de a provoca ionizarea.
Comparativ, particulele beta (electroni / positroni) sunt mai ușoare și pot călători mai repede. De asemenea, ele au jumătate din sarcina unei particule alfa. Aceasta înseamnă că puterea lor ionizantă este mai mică comparativ cu particulele alfa. De fapt, particulele beta pot fi oprite cu câteva milimetri de foi de aluminiu.
Fotonii emise de radiația gamma sunt descărcate și "fără masă". Pe măsură ce trec printr-un material, ei pot da energie electronilor care alcătuiesc materialul și provoacă ionizări. Totuși, puterea lor ionizantă este mult mai mică comparativ cu cea a alfa și beta. Pe de altă parte, aceasta înseamnă că capacitatea lor de a pătrunde în materiale este mult mai mare. Un bloc de plumb cu grosimea de cativa centimetri ar putea reduce intensitatea radiatiei gamma, dar chiar si acest lucru nu este suficient pentru a opri radiatia.
Graficul de mai jos compară unele dintre proprietățile radiațiilor alfa, beta și gamma
| Proprietate | Alfa radiații | Beta radiații | Gama de radiații |
| Natura particulei | Un nucleu de heliu | Un electron / pozitron | Un foton |
| Încărca |  |  | 0 |
| Masa |  |  | 0 |
| Viteza relativă | Încet | Mediu | Viteza luminii |
| Puterea ionizată relativă | Înalt | Mediu | Scăzut |
| Oprit de | Hârtie groasă de hârtie | Puține mm de foaie de aluminiu | (într-o oarecare măsură) O pereche de cm de bloc de plumb |
Referințe:
Particule de date Grup. (2013). Constante fizice. Recuperat la data de 24 iulie 2015, din grupul de date despre particule: http://pdg.lbl.gov/2014/reviews/rpp2014-rev-phys-constants.pdf
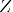 ): numărul de protoni din nucleul unui atom.
): numărul de protoni din nucleul unui atom.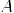 ): Numărul de nucleoni (protoni + neutroni) în nucleul unui atom.
): Numărul de nucleoni (protoni + neutroni) în nucleul unui atom.